(латинское Ferrum)
Fe, химический элемент VIII группы периодической системы Менделеева; атомный номер 26, атомная масса 55,847; блестящий серебристо-белый металл. Элемент в природе состоит из четырёх стабильных изотопов: 54Fe (5,84\%), 56Fe (91,68\%), 57Fe (2,17\%) и 58Fe (0,31\%).
Историческая справка. Ж. было известно ещё в доисторические времена, однако широкое применение нашло значительно позже, т. к. в свободном состоянии встречается в природе крайне редко, а получение его из руд стало возможным лишь на определённом уровне развития техники. Вероятно, впервые человек познакомился с метеоритным Ж., о чём свидетельствуют его названия на языках древних народов: древнеегипетское "бени-пет" означает "небесное железо"; древнегреческое sideros связывают с латинским sidus (родительный падеж sideris) - звезда, небесное тело. В хеттских текстах 14 в. до н. э. упоминается о Ж. как о металле, упавшем с неба. В романских языках сохранился корень названия, данного римлянами (например, французское fer, итальянское ferro).
Способ получения Ж. из руд был изобретён в западной части Азии во 2-м тысячелетии до н. э.; вслед за тем применение Ж. распространилось в Вавилоне, Египте, Греции; на смену бронзовому веку (См.
Бронзовый век) пришёл
Железный век. Гомер (в 23-й песне "Илиады") рассказывает, что Ахилл наградил диском из железной крицы победителя в соревновании по метанию диска. В Европе и Древней Руси в течение многих веков Ж. получали по сыродутному процессу (См.
Сыродутный процесс)
. Железную руду восстанавливали древесным углём в горне (см.
Восстановление металлов), устроенном в яме; в горн мехами нагнетали воздух, продукт восстановления - крицу ударами молота отделяли от шлака и из неё выковывали различные изделия. По мере усовершенствования способов дутья и увеличения высоты горна температура процесса повышалась и часть Ж. науглероживалась, т. е. получался
Чугун; этот сравнительно хрупкий продукт считали отходом производства. Отсюда название чугуна "чушка", "свинское
железо" - английское pig iron. Позже было замечено, что при загрузке в горн не железной руды, а чугуна также получается низкоуглеродистая железная крица, причём такой двухстадийный процесс (см.
Кричный передел) оказался более выгодным, чем сыродутный. В 12-13 вв. кричный способ был уже широко распространён. В 14 в. чугун начали выплавлять не только как полупродукт для дальнейшего передела, но и как материал для отливки различных изделий. К тому же времени относится и реконструкция горна в шахтную печь ("домницу"), а затем и в доменную печь. В середине 18 в. в Европе начал применяться тигельный процесс получения стали (См.
Сталь), который был известен на территории Сирии ещё в ранний период средневековья, но в дальнейшем оказался забытым. При этом способе сталь получали расплавлением металлические шихты в небольших сосудах (тиглях) из высокоогнеупорной массы. В последней четверти 18 в. стал развиваться пудлинговый процесс передела чугуна в Ж. на поду пламенной отражательной печи (см.
Пудлингование). Промышленный переворот 18 - начала 19 вв., изобретение паровой машины, строительство железных дорог, крупных мостов и парового флота вызвали громадную потребность в Ж. и его сплавах. Однако все существовавшие способы производства Ж. не могли удовлетворить потребности рынка. Массовое производство стали началось лишь в середине 19 в., когда были разработаны бессемеровский, томасовский и мартеновский процессы. В 20 в. возник и получил широкое распространение электросталеплавильный процесс, дающий сталь высокого качества.
Распространённость в природе. По содержанию в литосфере (4,65\% по массе) Ж. занимает второе место среди металлов (на первом алюминий). Оно энергично мигрирует в земной коре, образуя около 300 минералов (окислы, сульфиды, силикаты, карбонаты, титанаты, фосфаты и т. д.). Ж. принимает активное участие в магматических, гидротермальных и гипергенных процессах, с которыми связано образование различных типов его месторождений (см.
Железные руды). Ж. - металл земных глубин, оно накапливается на ранних этапах кристаллизации магмы, в ультраосновных (9,85\%) и основных (8,56\%) породах (в гранитах его всего 2,7\%). В биосфере Ж. накапливается во многих морских и континентальных осадках, образуя осадочные руды.
Важную роль в геохимии Ж. играют окислительно-восстановительные реакции - переход 2-валентного Ж. в 3-валентное и обратно. В биосфере при наличии органических веществ Fe3+ восстанавливается до Fe2+ и легко мигрирует, а при встрече с кислородом воздуха Fe2+ окисляется, образуя скопления гидроокисей 3-валентного Ж. Широко распространённые соединения 3-валентного Ж. имеют красный, жёлтый, бурый цвета. Этим определяется окраска многих осадочных горных пород и их наименование - "красно-цветная формация" (красные и бурые суглинки и глины, жёлтые пески и т. д.).
Физические и химические свойства. Значение Ж. в современной технике определяется не только его широким распространением в природе, но и сочетанием весьма ценных свойств. Оно пластично, легко куется как в холодном, так и нагретом состоянии, поддаётся прокатке, штамповке и волочению. Способность растворять углерод и др. элементы служит основой для получения разнообразных железных сплавов.
Ж. может существовать в виде двух кристаллических решёток: α- и γ- объёмноцентрированной кубической (ОЦК) и гранецентрированной кубической (ГЦК). Ниже 910 °С устойчиво α - Fe с ОЦК-решёткой (а = 2,86645 Å при 20°С). Между 910°С и 1400°С устойчива γ-модификация с ГЦК-решёткой (а = 3,64 Å). Выше 1400°С вновь образуется ОЦК-решётка δ-Fe (а = 2,94 Å), устойчивая до температуры плавления (1539°С). α - Fe ферромагнитно вплоть до 769°С (точка Кюри). Модификация γ-Fe и δ-Fe парамагнитны.
Полиморфные превращения Ж. и стали при нагревании и охлаждении открыл в 1868 Д. К.
Чернов. Углерод образует с Ж.
Твёрдые растворы внедрения, в которых атомы С, имеющие небольшой атомный радиус (0,77 Å), размещаются в междоузлиях кристаллической решётки металла, состоящей из более крупных атомов (атомный радиус Fe 1,26 Å). Твёрдый раствор углерода в γ-Fe наз.
Аустенитом, а в (α-Fe-
Ферритом.
Насыщенный твёрдый раствор углерода в γ
- Fe содержит 2,0\% С по массе при 1130°С; α-Fe растворяет всего 0,02- 0,04\%С при 723°С, и менее 0,01\% при комнатной температуре. Поэтому при закалке (См.
Закалка)
аустенита образуется
Мартенсит - пересыщенный твёрдый раствор углерода в α- Fe, очень твёрдый и хрупкий. Сочетание закалки с
Отпуском (нагревом до относительно низких температур для уменьшения внутренних напряжений) позволяет придать стали требуемое сочетание твёрдости и пластичности (см. Жел
езо - углеродистые сплавы (См.
Железоуглеродистые сплавы).
Термическая обработка металлов).
Физические свойства Ж. зависят от его чистоты. В промышленных железных материалах Ж., как правило, сопутствуют примеси углерода, азота, кислорода, водорода, серы, фосфора. Даже при очень малых концентрациях эти примеси сильно изменяют свойства металла. Так, сера вызывает т. н.
Красноломкость, фосфор (даже 10
-20\% Р) -
Хладноломкость; углерод и азот уменьшают
Пластичность, а водород увеличивает
Хрупкость Ж. (т. н. водородная хрупкость). Снижение содержания примесей до 10
-7-10
-9\% приводит к существенным изменениям свойств металла, в частности к повышению пластичности.
Ниже приводятся физические свойства Ж., относящиеся в основном к металлу с общим содержанием примесей менее 0,01\% по массе:
Атомный радиус 1,26 Å
Ионные радиусы Fe2+O,80 Å, Fe3+O,67 Å
Плотность (20oC) 7,874 г/см3
tпл 1539°С
tkип около 3200оС
Температурный коэффициент линейного расширения (20°С) 11,7·10-6
Теплопроводность (25°С) 74,04 вт/(м·К)
[0,177 (кал/см·сек·град)]
Теплоёмкость Ж. зависит от его структуры и сложным образом изменяется с температурой; средняя удельная теплоёмкость (0-1000oC) 640,57 дж/(кг·К) [0,153 кал/ (г·град)].
Удельное электрическое сопротивление (20°С)
9,7·10-8ом·м [9,7·10-6ом·см]
Температурный коэффициент электрического сопротивления
(0-100°С) 6,51·10-3
Модуль Юнга 190-210·103 Мн/м.2
(19-21·103кгс/мм2)
Температурный коэффициент модуля Юнга
4·10-6
Модуль сдвига 84,0·103 Мн/м2 [8,4·103кгс/мм2]
Кратковременная прочность на разрыв
170-210Мн/м2[17-21кгс/мм2]
Относительное удлинение 45-55\%
Твёрдость по Бринеллю 350-450 Мн/м2
[35-45 кгс/мм2]
Предел текучести 100Мн/м2 [10 кгс/мм2]
Ударная вязкость 300 Мн/м2 [30 кгс/мм2]
Конфигурация внешней электронной оболочки атома Fe 3
d64s2. Ж. проявляет переменную валентность (наиболее устойчивы соединения 2- и 3-валентного Ж.). С кислородом Ж. образует закись FeO, окись Fe
2O
3 и закись-окись Fe
3O
4 (соединение FeO с Fe
2O
3, имеющее структуру
Шпинели)
. Во влажном воздухе при обычной температуре Ж. покрывается рыхлой ржавчиной (Fe
2O
3·
nH
2O). Вследствие своей пористости ржавчина не препятствует доступу кислорода и влаги к металлу и поэтому не предохраняет его от дальнейшего окисления. В результате различных видов коррозии ежегодно теряются миллионы тонн Ж. (см.
Коррозия металлов). При нагревании Ж. в сухом воздухе выше 200°С оно покрывается тончайшей окисной плёнкой, которая защищает металл от коррозии при обычных температурах; это лежит в основе технического метода защиты Ж. - воронения (См.
Воронение)
. При нагревании в водяном паре Ж. окисляется с образованием Fe
3O
4 (ниже 570°С) или FeO (выше 570°С) и выделением водорода.
Гидроокись Fe (OH)2 образуется в виде белого осадка при действии едких щелочей или аммиака на водные растворы солей Fe2+ в атмосфере водорода или азота. При соприкосновении с воздухом Fe (OH)2 сперва зеленеет, затем чернеет и наконец быстро переходит в красно-бурую гидроокись Fe (OH)3. Закись FeO проявляет основные свойства. Окись Fe2O3 амфотерна и обладает слабо выраженной кислотной функцией; реагируя с более основными окислами (например, с MgO), она образует ферриты - соединения типа Fe2O3·nMeO, имеющие ферромагнитные свойства и широко применяющиеся в радиоэлектронике. Кислотные свойства выражены и у 6-валентного Ж., существующего в виде ферратов, например K2FeO4, солей не выделенной в свободном состоянии железной кислоты.
Ж. легко реагирует с галогенами и галогеноводородами, давая соли, например хлориды FeCl
2 и FeCl
3. При нагревании Ж. с серой образуются сульфиды FeS и FeS
2. Карбиды Ж. - Fe
3C (
Цементит)
и Fe
2C (ε-карбид) - выпадают из твёрдых растворов углерода в Ж. при охлаждении. Fe
3C выделяется также из растворов углерода в жидком Ж. при высоких концентрациях С. Азот, подобно углероду, даёт с Ж. твёрдые растворы внедрения; из них выделяются нитриды Fe
4N и Fe
2N. С водородом Ж. даёт лишь малоустойчивые гидриды, состав которых точно не установлен. При нагревании Ж. энергично реагирует с кремнием и фосфором, образуя силициды (например, Fe
3Si) и фосфиды (например, Fe
3P).
Соединения Ж. с многими элементами (О, S и др.), образующие кристаллическую структуру, имеют переменный состав (так, содержание серы в моносульфиде может колебаться от 50 до 53,3 ат.\%). Это обусловлено дефектами кристаллической структуры. Например, в закиси Ж. часть ионов Fe2+ в узлах решётки замещена ионами Fe3+; для сохранения электронейтральности некоторые узлы решётки, принадлежавшие ионам Fe2+, остаются пустыми и фаза (вюстит) в обычных условиях имеет формулу Fe0,947O.
Нормальный электродный потенциал Ж. в водных растворах его солей для реакции
составляет - 0,44 в, а для реакции
равен - 0,036
в. Т. о., в ряду активностей (См.
Ряд активностей) Ж. стоит левее водорода. Оно легко растворяется в разбавленных кислотах с выделением H
2 и образованием ионов Fe
2+.
Своеобразно взаимодействие Ж. с азотной кислотой (См.
Азотная кислота)
. Концентрированная HNO
3 (плотность 1,45
г/см3) пассивирует Ж. вследствие возникновения на его поверхности защитной окисной плёнки; более разбавленная HNO
3 растворяет Ж. с образованием ионов Fe
2+ или Fe
3+, восстанавливаясь до MH
3 или N
2O и N
2.
Растворы солей 2-валентного Ж. на воздухе неустойчивы - Fe
2+ постепенно окисляется до Fe
3+. Водные растворы солей Ж. вследствие
Гидролиза имеют кислую реакцию. Добавление к растворам солей Fe
3+ тиоцианат-ионов SCN
- даёт яркую кроваво-красную окраску вследствие возникновения Fe (SCN)
3, что позволяет открывать присутствие 1 части Fe
3+ примерно в 10
6 частях воды. Для Ж. характерно образование комплексных соединений (См.
Комплексные соединения)
. Получение и применение. Чистое Ж. получают в относительно небольших количествах электролизом водных растворов его солей или восстановлением водородом его окислов. Разрабатывается способ непосредственного получения Ж. из руд электролизом расплавов. Постепенно увеличивается производство достаточно чистого Ж. путём его прямого восстановления из рудных концентратов водородом, природным газом или углём при относительно низких температурах.
Ж. - важнейший металл современной техники. В чистом виде Ж. из-за его низкой прочности практически не используется, хотя в быту "железными" часто называют стальные или чугунные изделия. Основная масса Ж. применяется в виде весьма различных по составу и свойствам сплавов. На долю сплавов Ж. приходится примерно 95\% всей металлической продукции. Богатые углеродом сплавы (свыше 2\% по массе) - чугуны, выплавляют в доменных печах из обогащенных железных руд (см.
Доменное производство). Сталь различных марок (содержание углерода менее 2\% по массе) выплавляют из чугуна в мартеновских и электрических печах и конвертерах путём окисления (выжигания) излишнего углерода, удаления вредных примесей (главным образом S, Р, О) и добавления легирующих элементов (см.
Мартеновская печь, Конвертер). Высоколегированные стали (с большим содержанием никеля, хрома, вольфрама и др. элементов) выплавляют в электрических дуговых и индукционных печах. Для производства сталей и сплавов Ж. особо ответственного назначения служат новые процессы - вакуумный, электрошлаковый переплав, плазменная и электронно-лучевая плавка и др. Разрабатываются способы выплавки стали в непрерывно действующих агрегатах, обеспечивающих высокое качество металла и автоматизацию процесса.
На основе Ж. создаются материалы, способные выдерживать воздействие высоких и низких температур, вакуума и высоких давлений, агрессивных сред, больших переменных напряжений, ядерных излучений и т. п. Производство Ж. и его сплавов постоянно растет. В 1971 в СССР выплавлено 89,3 млн. т чугуна и 121 млн. т стали.
Л. А. Шварцман, Л. В. Ванюкова.
Железо как художественный материал использовалось с древности в Египте (подставка для головы из гробницы Тутанхамона около Фив, середина 14 в. до н. э., Музей Ашмола, Оксфорд), Месопотамии (кинжалы, найденные около Кархемиша, 500 до н. э., Британский музей, Лондон), Индии (железная колонна в Дели, 415). Со времён средневековья сохранились многочисленные высокохудожественные изделия из Ж. в странах Европы (Англии, Франции, Италии, России и др.) - кованые ограды, дверные петли, настенные кронштейны, флюгера, оковки сундуков, светцы. Кованые сквозные изделия из прутьев и изделия из просечного листового Ж. (часто со слюдяной подкладкой) отличаются плоскостными формами, чётким линейно-графическим силуэтом и эффектно просматриваются на свето-воздушном фоне. В 20 в. Ж. используется для изготовления решёток, оград, ажурных интерьерных перегородок, подсвечников, монументов.
Т. Л.
Жел
езо в организме. Ж. присутствует в организмах всех животных и в растениях (в среднем около 0,02\%); оно необходимо главным образом для кислородного обмена и окислительных процессов. Существуют организмы (т. н. концентраторы), способные накапливать его в больших количествах (например,
Железобактерии - до 17-20\% Ж.). Почти всё Ж. в организмах животных и растений связано с белками. Недостаток Ж. вызывает задержку роста и явления хлороза растений (См.
Хлороз растений)
, связанные с пониженным образованием
Хлорофилла
. Вредное влияние на развитие растений оказывает и избыток Ж., вызывая, например, стерильность цветков риса и хлороз. В щелочных почвах образуются недоступные для усвоения корнями растений соединения Ж., и растения не получают его в достаточном количестве; в кислых почвах Ж. переходит в растворимые соединения в избыточном количестве. При недостатке или избытке в почвах усвояемых соединений Ж. заболевания растений могут наблюдаться на значительных территориях (см.
Биогеохимические провинции).
В организм животных и человека Ж. поступает с пищей (наиболее богаты им печень, мясо, яйца, бобовые, хлеб, крупы, шпинат, свёкла). В норме человек получает с рационом 60-110
мг Ж., что значительно превышает его суточную потребность. Всасывание поступившего с пищей Ж. происходит в верхнем отделе тонких кишок, откуда оно в связанной с белками форме поступает в кровь и разносится с кровью к различным органам и тканям, где депонируется в виде Ж.- белкового комплекса - ферритина. Основное депо Ж. в организме - печень и селезёнка. За счёт Ж. ферритина происходит синтез всех железосодержащих соединений организма: в костном мозге синтезируется дыхательный пигмент
Гемоглобин, в мышцах -
Миоглобин, в различных тканях
Цитохромы и др. железосодержащие ферменты. Выделяется Ж. из организма главным образом через стенку толстых кишок (у человека около 6-10
мг в сутки) и в незначительной степени почками. Потребность организма в Ж. меняется с возрастом и физическим состоянием. На 1 кг веса необходимо детям - 0,6, взрослым - 0,1 и беременным - 0,3
мг Ж. в сутки. У животных потребность в Ж. ориентировочно составляет (на 1
кг сухого вещества рациона): для дойных коров - не менее 50
мг, для молодняка - 30-50
мг, для поросят - до 200
мг, для супоросных свиней - 60
мг. В. В. Ковальский.
В медицине лекарственные препараты Ж. (восстановленное Ж., лактат Ж., глицерофосфат Ж., сульфат 2-валентного Ж., таблетки Бло, раствор яблочнокислого Ж., ферамид, гемостимулин и др.) используют при лечении заболеваний, сопровождающихся недостатком Ж. в организме (железодефицитная анемия), а также как общеукрепляющие средства (после перенесённых инфекционных заболеваний и др.). Изотопы Ж. (52Fe, 55Fe и 59Fe) применяют как индикаторы при медико-биологических исследованиях и диагностике заболеваний крови (анемии, лейкозы, полицитемия и др.).
Лит.: Общая металлургия, М., 1967; Некрасов Б. В., Основы общей химии, т. 3, М., 1970; Реми Г., Курс неорганической химии, пер. с нем., т. 2, М., 1966; Краткая химическая энциклопедия, т. 2, М., 1963; Левинсон Н. Р., [Изделия из цветного и чёрного металла], в кн.: Русское декоративное искусство, т. 1-3, М., 1962-65; Вернадский В. И., Биогеохимические очерки. 1922-1932, М. - Л., 1940; Граник С., Обмен железа у животных и растений, в сборнике: Микроэлементы, пер. с англ., М., 1962; Диксон М., Уэбб Ф., ферменты, пер. с англ., М., 1966; Neogi P., Iron in ancient India, Calcutta, 1914; Friend J. N., Iron in antiquity, L.,1926; Frank E. B., Old French ironwork, Camb. (Mass.), 1950; Lister R., Decorative wrought ironwork in Great Britain, L., 1960.
Л. П. Катаев, В. П. Смирнов. Памятник пяти большевикам, расстрелянным в 1918 белогвардейцами, на Острове Залита (Псковское озеро).1967.
Ворота ограды церкви Вознесения в Коломенском (ныне в черте Москвы). 17 в.
Шкатулка из Великого Устюга. 18 в. Русский музей. Ленинград.
Дверная ручка и дверная петля-жиковина. 17 в.
Решетка ограды церкви Никиты Мученика в Москве. 18 в.
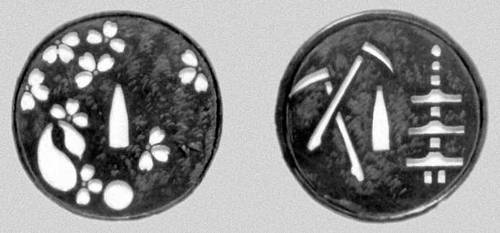
Цубы (пластины, отделяющие рукоятку меча от лезвия). 14-16 вв. Национальный музей. Токио.
Флюгер с Владимирской башни Китай-города в Москве. Конец 17 в. Исторический музей. Москва.
Решётка ограды дома Челлеси в Ареццо. 17 в.
Канделябр из Каталонии. 15 в. Музей Кау Феррат. Барселона.












![[[Диаграмма Пурбе]] для Fe-H<sub>2</sub>O [[Диаграмма Пурбе]] для Fe-H<sub>2</sub>O](https://commons.wikimedia.org/wiki/Special:FilePath/Pourbaix-fe.png?width=200)
