Перевод и анализ слов искусственным интеллектом ChatGPT
На этой странице Вы можете получить подробный анализ слова или словосочетания, произведенный с помощью лучшей на сегодняшний день технологии искусственного интеллекта:
- как употребляется слово
- частота употребления
- используется оно чаще в устной или письменной речи
- варианты перевода слова
- примеры употребления (несколько фраз с переводом)
- этимология
Что (кто) такое Зайцева реакция - определение
Википедия
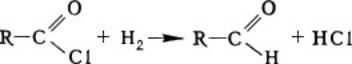
Реакция Розенмунда-Зайцева — селективное каталитическое восстановление ацилхлоридов водородом до альдегидов. Реакция была открыта М. М. Зайцевым в 1872 году, классическая вариация разработана Розенмундом в 1918.
В качестве катализатора обычно используют металлический палладий на носителе (BaSO4, CaCO3, ВаСО3, асбест, уголь, кизельгур), иногда Pt или Ni. Для предотвращения дальнейшего восстановления альдегидов в катализатор вводят контактные яды (фенилизотиоцианат, тетраметилтиомочевину, серу и др.). Реакцию проводят в орг. растворителе (бензоле, толуоле и др.), содержащем суспендир. катализатор, при 80-180°С. Реже используют парофазное гидрирование при 150—200°С. Выхода от хороших до превосходных. Часто в качестве побочных продуктов образуются спирты, углеводороды и сложные эфиры [образуются из спиртов и RC(O)Cl]. Также в реакционных смесях в следовых количествах обнаруживаются простые эфиры, ангидриды кислот, олигомеры и полимеры.

![А. М. Зайцев]] А. М. Зайцев]]](https://commons.wikimedia.org/wiki/Special:FilePath/Alexander Mikhaylovich Zaytsev.jpg?width=200)




