Введите слово или словосочетание на любом языке 👆
Язык:
Перевод и анализ слов искусственным интеллектом ChatGPT
На этой странице Вы можете получить подробный анализ слова или словосочетания, произведенный с помощью лучшей на сегодняшний день технологии искусственного интеллекта:
- как употребляется слово
- частота употребления
- используется оно чаще в устной или письменной речи
- варианты перевода слова
- примеры употребления (несколько фраз с переводом)
- этимология
Что (кто) такое Метастабильное состояние - определение
ТЕРМИН ОБОЗНАЧАЮЩИЙ СОСТОЯНИЕ СТАБИЛЬНОСТИ
Метастабильное состояние (в термодинамике); Метастабильное состояние квантовых систем; Неравновесная система; Метастабильность; Квазистационарное состояние
Метастабильное состояние
I
Метастаби́льное состоя́ние (от Мета... и лат. stabilis - устойчивый)
в термодинамике, состояние неустойчивого равновесия физической макроскопической системы, в котором система может находиться длительное время. Примерами М. с. могут служить перегретая или переохлажденная жидкость и переохлажденный (пересыщенный) пар (см. Перегрев и Переохлаждение). Жидкость, например воду, тщательно очищенную от посторонних твёрдых частичек и пузырьков газа (центров парообразования), можно нагреть до температуры, превышающей температуру кипения при данном давлении. Если в перегретой жидкости возникнут центры парообразования (или их введут искусственно), то жидкость взрывообразно перейдёт в пар - устойчивое при данной температуре состояние. В свою очередь пар, в котором отсутствуют центры конденсации (твёрдые частицы, ионы), можно охладить до температур, при которых устойчиво жидкое состояние, и получить переохлажденный (пересыщенный) пар. В природе пересыщенный водяной пар образуется, например, при подъёме нагретых у поверхности земли воздушных масс и последующем их охлаждении, вызванном адиабатическим расширением.
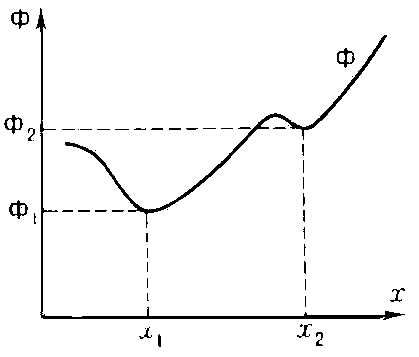
Возникновение М. с. объясняется теорией термодинамического равновесия (см. Равновесие термодинамическое). Состоянию равновесия замкнутой системы соответствует максимум энтропии (См. Энтропия) S. При постоянном объёме V и температуре Т равновесию отвечает минимум свободной энергии F (гельмгольцевой энергии (См. Гельмгольцева энергия)), а при постоянном давлении р и температуре Т - минимум термодинамического потенциала G (гиббсовой энергии (См. Гиббсова энергия)). Однако определённым значениям внешних параметров (р, V, Т и др.) может соответствовать несколько экстремумов (максимумов или минимумов) одной из перечисленных выше функций (рис.). Каждому из относительных минимумов функции F или G соответствует устойчивое по отношению к малым воздействиям или флуктуациям (См. Флуктуации) состояние. Такие состояния называют метастабильными. При небольшом отклонении от М. с. система возвращается в это же состояние, однако по отношению к большим отклонениям от равновесия она неустойчива и переходит в состояние с абсолютным минимумом термодинамического потенциала, которое устойчиво по отношению к конечным отклонениям значений физических параметров от равновесных. Т. о., хотя М. с. в известных пределах устойчиво, рано или поздно система всё же переходит в абсолютно устойчивое, стабильное состояние.
Возможность реализации М. с. связана с особенностями перехода системы из одного устойчивого состояния в другое (с кинетикой фазовых переходов (См. Фазовый переход)). Фазовый переход начинается с возникновения зародышей новой фазы: пузырьков пара в случае перехода жидкости в пар, микрокристалликов при переходе жидкости в кристаллическое состояние и т.п. Для образования зародышей требуется совершение работы по созданию поверхностей раздела двух фаз. Росту образовавшихся зародышей мешает значительная кривизна их поверхности (см. Капиллярные явления), приводящая при кристаллизации к повышенной растворимости зародышей твёрдой фазы, при конденсации жидкости - к испарению мельчайших капелек, при парообразовании - к повышенной упругости пара внутри маленьких пузырьков. Указанные факторы могут сделать энергетически невыгодным возникновение и рост зародышей новой фазы и задержать переход системы из М. с. в абсолютно устойчивое состояние при данных условиях.
М. с. широко встречаются в природе и используются в науке и технике. С существованием М. с. связаны, например, явления магнитного, электрического и упругого Гистерезиса, образование пересыщенных растворов, Закалка стали, производство стекла (См. Стекло) и т.д.
Лит.: Ландау Л. Д., Лифшиц Е. М., Статистическая физика, М., 1964; Штрауф Е. А., Молекулярная физика, М. - Л., 1949; Самойлович А. Г., Термодинамика и статистическая физика, 2 изд., М., 1955; Скрипов В. П., Метастабильная жидкость, М., 1972.
Г. Я. Мякишев.
Ф1(х1) - абсолютный минимум функции Ф (ею могут быть потенциалы F или G), Ф2(х2) - относительный минимум функции; х - переменный физический параметр (например, объём V), другие параметры постоянны.
II
Метастаби́льное состоя́ние
квантовых систем, возбуждённое состояние атомных систем (атомов, молекул, атомных ядер), которые могут существовать длительное время и, т. о., стабильны. Метастабильными являются такие возбуждённые состояния, Квантовые переходы из которых в состояния с меньшей энергией, сопровождающиеся излучением (т. е. испусканием фотонов), запрещены Отбора правилами (точными или приближёнными) и, следовательно, либо совсем не могут происходить, либо мало вероятны. Мера метастабильности состояния - его время жизни τ = 1/A, где А - полная вероятность перехода из данного состояния во все состояния с меньшей энергией. Чем меньше А, тем больше τ и тем состояние более стабильно. В предельном случае строго запрещенных переходов А = 0, τ = ∞. Обычно времена жизни для М. с. атомов и молекул составляют доли сек и сек.
Атомы и молекулы в М. с. играют важную роль в элементарных процессах, например в разрежённых газах: энергия возбуждения может длительное время сохраняться частицами, находящимися в М. с., и затем передаваться другим частицам при столкновении, что вызывает послесвечение. Процессы люминесценции (См. Люминесценция) сложных молекул связаны с наличием метастабильных молекул в триплетных возбуждённых состояниях, переходы из которых в основное синглетное состояние запрещены правилами отбора. О М. с. ядер см. Изомерия атомных ядер.
М. А. Ельяшевич.
МЕТАСТАБИЛЬНОЕ СОСТОЯНИЕ
относительно устойчивое состояние системы, из которого она может перейти в более устойчивое состояние под действием внешних факторов или самопроизвольно (в последнем случае вероятность перехода значительно меньше, чем для нестабильного состояния). Пример метастабильного состояния в термодинамике - жидкость в состоянии перегрева или переохлаждения; метастабильное состояние в квантовой механике - возбужденные состояния атомов, молекул или атомных ядер, в которых они могут находиться длительное время.
Метастабильное состояние
Метастабильное состояние (от «через» и «устойчивый») — состояние квазиустойчивого равновесия физической системы, в котором система может находиться длительное время.
Википедия
Метастабильное состояние
Метастабильное состояние (от греч. μετα «через» и лат. stabilis «устойчивый») — состояние квазиустойчивого равновесия физической системы, в котором система может находиться длительное время.
Что такое метастабильное состояние, может быть понятно из приведенного справа рисунка:
- состояние 1: метастабильное — состояние, стабильность которого сохраняется при не очень больших возмущениях;
- состояние 2: нестабильное — состояние, стабильность которого нарушается при сколь угодно малых возмущениях;
- состояние 3: стабильное — состояние, стабильность которого сохраняется при больших возмущениях.
Метастабильные состояния широко встречаются в природе и используются в науке и технике. С существованием метастабильных состояний связаны, например, явления магнитного, электрического и упругого гистерезиса, образование перенасыщенных растворов, закалка стали, производство стекла и т. д.

